Monitorage du
segment ST :
Quel place en 2001 ?.
Dr Christophe Decoene

Service d’Anesthésie-Réanimation en Cardiologie Clinique de chirurgie CardioVasculaire CHRU Lille
| Titre |
Monitorage du
segment ST : |
| Auteur |
Dr Christophe Decoene |
 |
Service d’Anesthésie-Réanimation en Cardiologie Clinique de chirurgie CardioVasculaire CHRU Lille |
Les modifications électriques induites par l’ischémie entraînent une modification de l’électrocardiogramme et notamment du segment ST. La détection de ces modifications a été utilisée lors des épreuves d’effort par les cardiologues (Blackburn 1969) et a permis les premiers dépistages de la maladie coronarienne. En 1976, Dalton et coll. ont décrit la premičre utilisation de cette surveillance dans le cadre de la surveillance d’une anesthésie générale. L’amélioration des technologies a permis une analyse informatisée des modifications du segment ST autorisant ainsi une surveillance en continu de ce segment. En 1979, Roy et coll. décrivirent la premičre analyse informatisée de ce monitorage1. En 1984, Kotrly et al présentent un systčme de monitorage compatible avec une utilisation en routine notamment grâce ŕ un moyennage des électrocardiogrammes et des modifications du segment ST dans le temps2. Depuis lors, ce monitoring a été intégré en options ŕ de nombreux moniteurs d’anesthésie et de réanimation. L’arrivée de nouvelles techniques d’évaluation de l’ischémie péri-opératoire et les améliorations concernant la prise en charge des patients coronariens ont-elles modifié la place de ce monitorage en l’an 2001.
Le segment ST correspond au temps pendant lequel l’ensemble des cellules myocardiques sont dépolarisées. Ce segment est normalement isoélectrique. L’ischémie coronarienne entraîne la persistance d’une activité électrique du territoire en souffrance et l’apparition d’un potentiel électrique négatif ou positif au cours de ce temps. Cette différence de potentiel est convertie en millimčtre (0.1mV = 1 mm) en raison de l’édition historique sur papier millimétré de l’électrocardiogramme. Cette convention a été conservée par la suite pour le monitorage.
Les termes de sus et sous décalage sont définis en fonction de la position du segment par rapport ŕ la ligne isoélectrique.
Pour ętre symptomatique d’une ischémie, il est nécessaire que le potentiel du segment ST soit > ou < ŕ 0,1 mV (soit plus ou moins 1 mm) et d’une durée supérieure ŕ 20 sec ou présent sur 10 complexe consécutifs. La sus ou sous dénivellation du segment ST pour ętre le reflet d’une ischémie myocardique doit également remplir les conditions suivantes : en présence d’un sous décalage rectiligne l’amplitude doit ętre de - 0,1 mV (- 1 mm), en cas de sous décalage descendant le point J doit ętre négatif de plus de – 0,1 mV (-1 mm), en présence d’un sus décalage celui-ci doit s’accompagner d’une élévation 80 ms aprčs le point J de plus de 2 mm pour ętre symptomatique d’une ischémie 3
Le recueil papier permet une lecture directe du segment ŕ la différence du recueil Holter ou ŕ l’aide de moniteur qui nécessitent un traitement informatisé du signal. Le signal ECG est un signal constitué de nombreux signaux de fréquence et d’amplitude différentes. Tout phénomčne possédant une variation sinusoďdale peut parasiter le recueil du signal. Le moniteur et le Holter vont recueillir l’ensemble des phénomčnes électriques sinusoďdaux ŕ la surface de la peau. Pour en dégager un signal ECG correct et non parasité il est nécessaire d’éliminer certaines fréquences ŕ l’aide de filtres. Ceci va limiter la qualité du recueil et ainsi masquer ou amplifier des modifications du segment ST. La qualité du recueil est également liée ŕ l’utilisation d’électrodes cutanées de faible impédance sur une peau bien dégraissée et ŕ l’aide de câbles bien isolés.
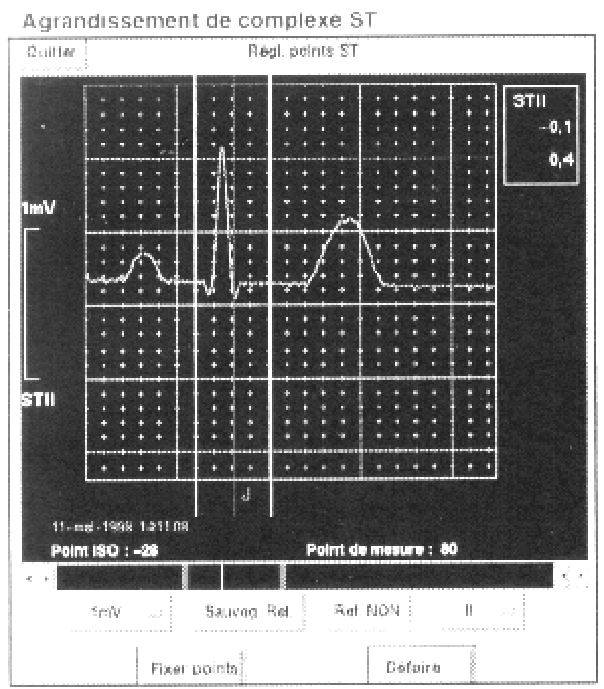
Pour déterminer l’existence d’un potentiel il est nécessaire de définir un point isoélectrique de référence, celui-ci est par convention détecté avant le complexe QRS en rčgle générale 30 ms avant l’activation ventriculaire (espace PR absence de dépolarisation cellulaire pendant la conduction auriculo-ventriculaire). La différence de potentiel électrique du segment ST par rapport ŕ ce point isoélectrique est alors mesuré en rčgle générale 80 ms aprčs la fin du complexe QRS (point J). Il est ainsi mesuré une différence en mV entre ces deux points de référence1,3. Il est ŕ noter que pour le Holter comme pour les nouveaux moniteurs ces points peuvent ętre modifiés en fonction des conditions rythmiques (Figure 1)
Les modifications du segment ST observées dans une dérivation témoignent de l’ischémie coronarienne dans le territoire exploré par la dérivation. Il est théoriquement possible de monitorer l’ensemble du massif myocardique ŕ l’aide de dérivations uni ou bipolaires (12 ou 15). Il faut souligner que la détection dans une des dérivations ne fournit pas de renseignements sur l’artčre coronaire atteinte (75 % des épisodes ischémiques sont observés en V5 quelque soit le lieu de l’atteinte coronaire). Les multiplications des dérivations permettent d ‘amplifier les chances de dépister l’ischémie myocardique. L’association DII et V5 détecte 80% des modifications et l’association DII, V4, V5 permet de diagnostiquer 96% des épisodes ischémiques3. Ces notions sont importantes pour optimiser une surveillance sans amplifier le nombre de paramčtres ŕ surveiller.
Si l’ischémie coronarienne se traduit par une modification électrique du segment ST toute modification du segment ST n’est pas symptomatique d’une ischémie coronarienne. En dehors des artéfacts de recueil il faut souligner l’existence d’anomalies non ischémiques du segment ST. Les situations les plus fréquentes sont les suivantes : la présence d’un bloc de branche (gauche en particulier), ce bloc de branche peut apparaître au cours d’une tachycardie, la présence d’une stimulation ventriculaire (pacemaker), la présence d’une hypokaliémie (calcémie, magnésémie), la prise de digitaliques, une hypertrophie ventriculaire gauche importante, une onde r de faible amplitude, les perturbations glycémiques, l’hypocapnie, l’existence d’une hémorragie méningée, lors de césariennes, de stimulation adrénergique ou chez un sujet jeune vagotonique1,3.
La méthode de référence est l’ECG de surface
La méthode de référence de recueil du segment ST est l’enregistrement papier et l’analyse directe sur papier millimétré de la modification de ce segment. Malheureusement cette technique n’est utilisable que sur une courte durée et non pas pour un monitorage de plusieurs heures voire de plusieurs jours.
L’enregistrement Holter
Des systčmes d’analyse automatisée du segment ST ont été mis au point. Ceux-ci permettent une analyse sur plusieurs jours et réalisent ainsi un enregistrement continu du segment ST. Cette analyse est trčs proche de l’analyse obtenue par une lecture papier directe, elle comporte néanmoins des risques d’erreurs notamment par digitalisation des modifications du segment ST. Il permet une analyse sur 12 dérivations un monitorage sur plus de 72 heures voir en ambulatoire. Une analyse battement par battement peut ętre réalisée a posteriori. La faible disponibilité des enregistreurs Holter ne permet leur utilisation ŕ une grande échelle pour la surveillance de l’ensemble des patients en périopératoire.
Le monitorage automatisé continu du segment ST pour l’anesthésie, la réanimation et ou les soins intensifs (MAC-ST pour cette communication)
Le signal ECG obtenu sur le cardioscope peut ętre analysé pour permettre une mesure du segment ST. Cette analyse nécessite des logiciels spécifiques et des précautions d’emploi particuličres. L’utilisation d’un filtre de fréquences est fréquente au bloc opératoire pour éliminer du recueil ECG l’ensemble des phénomčnes sinusoďdaux parasites qui viennent perturber le recueil de l’activité électrique myocardique soit en s’y additionant soit en modifiant son amplitude (parmi celles-ci on peut citer le réseau électrique 50 hertz , le bistouri électrique, la fréquence respiratoire 0.25 ŕ 0.1 hertz, les pompes ect…). Le but est d’obtenir un signal ECG lissé et pur pour la détection du rythme cardiaque et de ses troubles. La surveillance du segment ST a contrario requiert un filtrage minimum et une large bande passante de 0.04 ŕ 50 hertz. Ceci explique la sensibilité aux artéfacts de l’électrocardioscope en mode de surveillance du segment ST. Ce parasitage rend parfois impossible la surveillance de ce męme segment ST. Il en va de męme avec l’atténuation de l’amplitude du signal qui peut modifier artificiellement la position du segment ST par rapport ŕ la ligne isoélectrique. La plupart des moniteurs possčdent plusieurs modes d’analyse du signal ECG un mode monitoring peu utile pour l’analyse du ST et un mode diagnostic permettant une analyse du ST optimale. La surveillance du segment ST nécessite le monitorage de plusieurs dérivations pour ne pas ętre faussement rassurant. Le Holter et l’enregistrement papier permettent un enregistrement de plus de 12 dérivations tandis que le MAST en rčgle générale ne permet que la surveillance de trois dérivations, certains jusqu’ŕ 12. Cela est liée ŕ la puissance des logiciels ou ŕ leur configuration mais également aux possibilités parfois limitées de dérivations accessibles en raison du champ chirurgical. L’utilisation de deux dérivations (DII et V5) permet un dépistage de plus de 80% des modifications électriques observées sur 12 dérivations, l’ajout d’une dérivation n’augmente que de peu cette sensibilité. L’utilisation d’un câble ŕ trois branches permet également une surveillance du segment ST. Un placement particulier des électrodes permet alors d’obtenir un équivalent des dérivations ŕ surveiller. 1,3
L’intéręt d’un quelconque monitorage est de dépister précocement le risque et d’éviter les complications sans multiplier les interventions thérapeutiques par un manque de spécificité. La détection de l’ischémie coronarienne pose encore en l’an 2001 le problčme d’une détection délicate. Seules la surveillance du segment ST, la surveillance d’anomalies de cinétique segmentaire (ETO, Cardiokimographie), et la détection de troponine circulante permettent d’évoquer une ischémie myocardique. La détection de la troponine circulante est la seule méthode spécifique ŕ 100%, malheureusement elle témoigne d’une ischémie non réversible et son élévation est trop tardive pour en faire un élément de diagnostic précoce. La diminution du débit coronarien entraîne l’apparition d’anomalies de la cinétique segmentaire de la région myocardique hypoperfusée. La quantification de ces anomalies est trčs aléatoire, nécessite souvent des opérateurs entraînés et est rendue difficile par la préexistence d’anomalies de la cinétique segmentaire ou globale. D’autre part des anomalies de la cinétique segmentaire peuvent exister en l’absence d’ischémie vraie. Les problčmes liés ŕ la surveillance du segment ST ont été exposés auparavant.
Le monitorage du ST a souligné l’absence de relation entre les variations hémodynamiques et l’apparition de modification du segment ST cette discordance a également été mise en évidence par les autres moyens de détection de l’ischémie. En 1989, Mangano et coll mettaient en évidence que plus de 60% des épisodes ischémiques étaient indépendants de toutes variations hémodynamiques dans la phase opératoire et que parmi tous les paramčtres hémodynamiques la tachycardie était probablement la variable la mieux corrélée ŕ des modifications du segment ST 4-6
L’état du réseau coronaire est également un facteur qui modifie les variations observées du segment ST, Hogue et collaborateurs ont montré que les modifications du segment ST étaient plus fréquentes et plus durables chez les patients coronariens au réseau de suppléance médiocre en préopératoire7. Cette étude souligne ainsi la relation entre la délivrance en oxygčne et les modifications du segment ST. Les risques d’ischémie peropératoire sont reliés plus ŕ un défaut de délivrance d’oxygčne qu’ŕ une augmentation des besoins.
Les modifications du segment ST de longue durée et répétées sont responsables d’une production de troponine en postopératoire. Rapp et coll. rapportent en chirurgie vasculaire lourde la détection de troponine lors d’épisodes répétés et soutenus de modifications du segment ST. L’absence d’élévation de la troponine lors d’événements peu répétés et de courte durée laisse suggérer que des ischémies myocardiques męme importantes mais de courtes durées non pas le męme pronostic qu’une ischémie modérée mais persistante8. Cette étude vient conforter la spécificité du monitorage du segment ST pour la détection de l’ischémie myocarde et souligne les situations ŕ risque de nécrose myocardique. Dans les années 1985 et 1986 Slogoff et Keats ont montré une relation nette entre la détection d’événements ischémiques périopératoires et la survenue d’un infarctus du myocarde chez les patients opérés d’une revascularisation coronarienne. Cette relation a été confirmée depuis mais le plus souvent en chirurgie de revascularisation coronarienne4-7. Pour la chirurgie non cardiaque, il existe peu d’études prouvant l’impact des MAC-ST lors des périodes périopératoires sur le devenir des patients. Souvent au cours de ces études la surveillance du segment ST est réalisée pour analyser tel type de technique d’anesthésie ou bien tel protocole de prise en charge. C’est ainsi que lors de la chirurgie vasculaire Garnett et coll mettent en évidence l’absence de différence entre l’anesthésie générale et l’anesthésie locorégionale en termes d’épisodes d’ischémie. Cette étude a comme intéręt de souligner les périodes ŕ risque d’ischémie coronarienne que sont les tractions sur le mésentčre et les gestes de soins notamment la toilette en postopératoire, et une fréquence d’infarctus plus importante dans le groupe présentant des modifications peropératoires du segment ST9.
L’atteinte ischémique post-opératoire est sous estimée car mal surveillée or il semble que l’intéręt du monitorage du segment est probablement supérieur dans la phase postopératoire que peropératoire comme le souligne Mangano4. Cette męme mise en garde est attestée par L Landesberg10 qui souligne le risque majeur d’une ischémie myocardique sous-endocardique prolongée postopératoire
Pour permettre de définir son choix en vue de l’acquisition de tel ou tel matériel il est impératif de mener des comparaisons entre les différents moyens de surveillance en prenant en considérations leurs avantages et leurs inconvénients.
En rčgle générale les valeurs obtenues par le MAC-ST sont supérieures ŕ celles obtenues pour le męme patient ŕ l’aide du Holter ou sur l’ECG de surface11. Ce phénomčne est plus en rapport avec la distorsion du signal qu’avec une détection plus fiable de l’ischémie. Ceci souligne la nécessité de moduler les sous ou sus décalages de faible amplitude. Ansley a montré une sensibilité de 74% et une spécificité de 92% pour un MAC-ST Marquette 700012.
Les différents logiciels MAC-ST comparés entre eux présentent des capacités différentes de détection de l’ischémie coronarienne comparée au Holter. Leung a ainsi étudié le Marquette Tramscope 12C, le Datex AS/3 et le HPMerlin M1175A/M1176A. Leur sensibilité et spécificité respectives étaient les suivantes (75% et 89%, 60% et 69%, 78% et 71 %). L’auteur concluait sur la nécessité d’obtenir des tracés papiers pour contrôler les modifications observées sur les MAC-ST13.
La concordance ETO-ST pour la détection de l’ischémie myocardique est faible. Selon Communale et coll, la sensibilité de l’ETO serait deux fois plus importante que le monitoring du segment ST mais cela au prix d’une spécificité diminuée14-17. Cette absence de concordance avait déjŕ été soulignée par London et coll, ce męme auteur soulignait que les altérations sous formes d’akinésie ou de dyskinésies étaient plus prédictives que l’apparition d’une hypokinésie15. Malheureusement l’emploi systématique et continu de l’ETO est difficile en périopératoire pour la surveillance de l’ischémie.
On peut définir deux grands types d’indications pour la surveillance du segment ST. Le patient coronarien, la chirurgie lourde (chirurgie vasculaire, abdominale lourde ou hémorragique). Cette surveillance ne doit pas ętre uniquement peropératoire mais doit se prolonger dans la période postopératoire (3 ŕ 5 jours)4
La surveillance automatisée du segment ST malgré l’ensemble de ces pičges reste l’unique moyen de détection aisée des épisodes d’ischémie coronarienne périopératoire. De nombreuses études ont souligné le bénéfice d’une surveillance accrue et optimisée des patients pendant la période périopératoire. Il est probable que la surveillance ŕ l’aide du monitoring du segment ST contribue ŕ améliorer le devenir de nos patients. Malheureusement cet effet est impossible ŕ mettre en évidence. La survenue des épisodes ischémiques en dehors de tout signe hémodynamique (ischémie silencieuse) justifie ŕ elle-męme le monitorage du segment ST. La seule restriction ŕ son utilisation est la nécessité d’une parfaite connaissance de ses limites.
1 Kaplan et Thys, Electrocardiography in Anesthesia Miller 1987; Vol I, 1121-27
2 Kotrly et al Anesth Analg 1984;63:343-45
3 Lehot et coll Ischémie myocardique et Anesthésie Ann Fra Anesth 1995;14:1746-1974 Mangano et al JACC 1991; 17:843-57
5 Slogoff and Keats Anesthesiology 1985; 62 :107-1146 Urban et al Anesth Analg 1993 ;76 :942-97 Hoghe et al Anesthesiology 1993;79:514-24
8 Rapp et al Acta Anaesthesiol Scand 1999 ;43 : 124-299 Garnett et al Can J Anaesth 1996;43:769-77
10 Landesberg Lancet, 1993 ; 341 : 715-1911 Slogoff et al Anesthesiology 1990 ;73 :1074-8112 Ansley et al Can J Anesth 1996;43:995-1000
13 Leung et al. Anesth Analg 1998; 87:4-10
14 Communale et al Anesthesiology 1998 ;88 :945-5415 Leung et al eto Anesthesiology 1990 ;73 :802-81416 Smith et al Circulation 1985;5:1015-21
17 London et al Anesthesiology 1990 ;73 :644-55